- La frecuencia de la radiación (fotón) debe ser la adecuada para permitir la transición entre estados vibracionales. Dicho de otro modo, la frecuencia de la radiación debe coincidir con la frecuencia natural del movimiento vibracional.
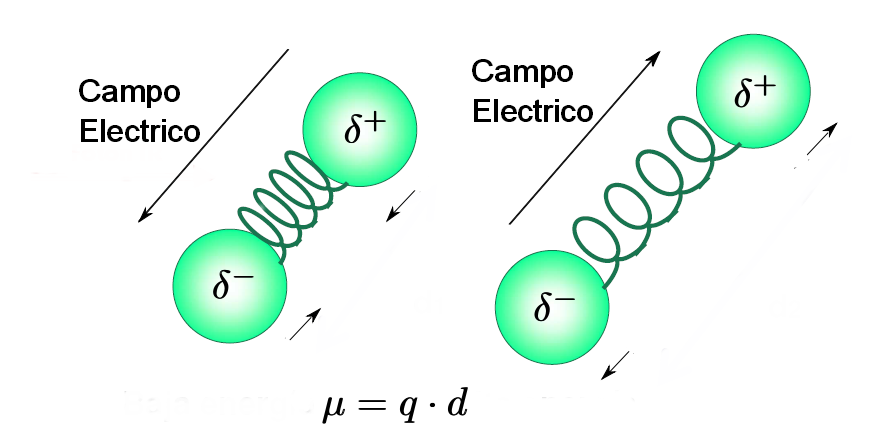
- Una molécula sólo absorbe radiación infrarroja cuando su momento dipolar interacciona con el campo eléctrico de la onda, variando en fase con este. Como es lógico este acoplamiento sólo es posible si las frecuencias de la radiación y la vibración del enlace coinciden. Por ello, moléculas apolares no absorben en el infrarrojo y moléculas poco polares dan lugar a absorciones muy débiles.
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?

