 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
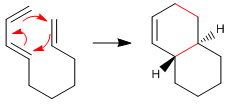
La reacción de Diels-Alder Intramolecular (IMDA) es una poderosa variante de la cicloadición [4+2] en la que el dieno y el dienófilo no son moléculas separadas, sino que forman parte de la misma molécula.
Ambas mitades reactivas están conectadas por una cadena (o "tether"), generalmente de átomos de carbono, aunque puede incluir heteroátomos (O, N, Si). La reacción, típicamente inducida por calor, provoca que la molécula se "pliegue" sobre sí misma para formar un sistema bicíclico o policíclico en un solo paso.
Ventajas Clave de la IMDA
La naturaleza intramolecular de esta reacción le confiere ventajas significativas sobre su contraparte intermolecular:
- Ventaja Entrópica (Cinética): Al estar el dieno y el dienófilo "atados", la pérdida de entropía de traslación en el estado de transición es mucho menor. Los reactivos ya están en alta proximidad (alta "concentración efectiva"). Esto hace que la reacción sea cinéticamente mucho más rápida y, a menudo, requiera temperaturas más bajas.
- Alto Control Regio- y Estereoquímico: La estructura y longitud de la cadena de conexión (tether) pre-organiza el estado de transición. Esto elimina la ambigüedad regioquímica (no hay productos "orto" vs "meta", solo hay una forma de unirse) y ejerce un control estereoquímico absoluto sobre el producto.
- Eficiencia Sintética: Es una de las herramientas más potentes en síntesis orgánica para construir esqueletos policíclicos complejos (como los encontrados en esteroides, alcaloides y otros productos naturales) de manera rápida y elegante.
Factores que Controlan la Reacción
A. Longitud del "Tether" (Cadena de Conexión)
Este es el factor más crítico. La longitud de la cadena determina la facilidad de la ciclación y el tamaño de los anillos formados.
- Tethers de 3 o 4 átomos: Son los más comunes y eficientes. Conducen a estados de transición energéticamente favorables (tipo silla) que forman anillos fusionados de 5 o 6 miembros (ej. sistemas 6/5 o 6/6).
- Tethers cortos (1 o 2 átomos): Generalmente no reaccionan, ya que implicarían una tensión angular extrema (anillos de 3 o 4 miembros) en el estado de transición.
- Tethers largos (5+ átomos): La reacción se vuelve más lenta (mayor coste entrópico para encontrar la conformación reactiva) y puede empezar a competir con reacciones intermoleculares (dímeros).
B. Estereoquímica del Producto (Sistemas Fusionados vs. Puenteados)
La topología del producto (cómo se conectan los anillos) depende de cómo esté conectada la cadena al dieno y al dienófilo.
- Formación de Sistemas Fusionados (Fused): Ocurre cuando el tether conecta el extremo del dieno (C4) con el dienófilo. Es el modo más común y da lugar a sistemas como hidrindanos (fusión 6/5) o decalinas (fusión 6/6).
- Formación de Sistemas Puenteados (Bridged): Ocurre cuando el tether conecta una posición interna del dieno (C2 o C3) con el dienófilo. Esto genera estructuras tipo norborneno, que son más tensas pero sintéticamente valiosas.
Además, la geometría (E/Z) de los dobles enlaces en la cadena y la estereoquímica de los sustituyentes en el tether dictan de forma predecible la estereoquímica relativa de los centros quirales recién formados en el producto bicíclico.
YouTube | Miembros del canal Hazte miembro del canal para acceder a todos los vídeos Vídeos para miembros