 En la actualidad se conocen más de 30 millones de compuestos químicos, de los cuales 1 millón son inorgánicos y el resto orgánicos. Los químicos determinan las propiedades físicas y químicas de estas sustancias (puntos de fusión y ebullición, solubilidad, densidad....). Sin embargo, la información más codiciada por el químico es la determinación de la estructura del compuesto, qué tipo de átomos lo forman y cómo se enlazan dichos átomos.
En la actualidad se conocen más de 30 millones de compuestos químicos, de los cuales 1 millón son inorgánicos y el resto orgánicos. Los químicos determinan las propiedades físicas y químicas de estas sustancias (puntos de fusión y ebullición, solubilidad, densidad....). Sin embargo, la información más codiciada por el químico es la determinación de la estructura del compuesto, qué tipo de átomos lo forman y cómo se enlazan dichos átomos.
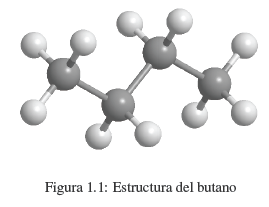
Sabemos que una sustancia como el butano está formada por carbono e hidrógeno. Cada molécula contiene 4 átomos de carbono y 10 átomos de hidrógeno, lo cual se representa mediante la fórmula C4H10, llamada fórmula molecular. Además sabemos que los átomos de carbono se enlazan formando una cadena lineal. Al primer carbono se unen 3 hidrógenos, al segundo carbono 2 hidrógenos, al tercer carbono 2 hidrógenos y al cuarto carbono los últimos 3 hidrógenos.
 ¿Cómo obtienen los químicos esta información?. Desafortunadamente no existe un microscopio capaz de distinguir los átomos y ver como se unen para formar la molécula. A continuación, se inician los pasos a seguir:
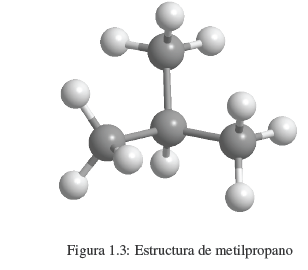
¿Cómo obtienen los químicos esta información?. Desafortunadamente no existe un microscopio capaz de distinguir los átomos y ver como se unen para formar la molécula. A continuación, se inician los pasos a seguir:- Determinar la fórmula molecular, que puede realizarse mediante la espectrometría de masas de alta resolución (HRMS). Aunque existen métodos clásicos que permiten determinar la formula molecular a partir de la composición centesimal y peso molecular del compuesto. En este momento, conocemos los átomos que componen nuestro compuesto y la proporción en la que participan. En el caso del butano, C4H10. Una vez conocida la fórmula molecular podemos escribir las posibles estructuras del compuesto. La fórmula C4H10 es compatible con dos isómeros: butano lineal y metilpropano.
- Una vez consideradas las posibles estructuras de nuestra fórmula molecular, el análisis de los espectros permitirá distinguir unos isómeros de otros para establecer cual de ellos corresponde a la sustancia problema.


