¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
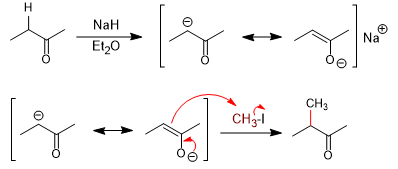
Los hidrógenos vecinos al grupo carbonilo de aldehídos, cetonas, ésteres, amidas, nitrilos, nitrocompuestos...., presentan una notable acidez, pudiendo ser sustraídos con bases fuertes, para dar lugar a los respectivos enolatos. La acidez de estos hidrógenos es causada por la combinación del efecto inductivo y resonante del grupo carbonilo, capaces de estabilizar la carga generada por la sustracción del hidrógeno.
No todos los grupos poseen la misma capacidad para estabilizar la carga, siendo el grupo nitro uno de los más efectivos, dando lugar a valores de pKa para sus hidrógenos alfa de 10.
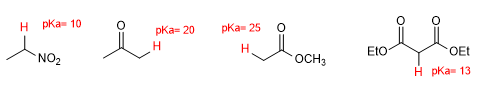
Los efectos de estos grupos se suman, así, el malonato de dietilo presenta hidrógenos alfa con pKa de 13; el acetilacetato de etilo de 11; y el propranodial de 9.
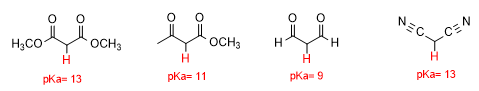
La fuerte estabilización por resonancia del malonato de dimetilo o del acetilacetato de metilo explica los valores tan bajos de pKa de sus respectivos hidrógenos alfa.
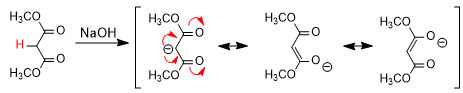
Los enolatos participan en numerosas reacciones de los compuestos carbonilos, como la condensación aldólica, la reacción de Michael o reacciones de alquilación como la mostrada a continuación.