 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
Los fotones de radiación infrarroja son absorbidos por los enlaces de una molécula pasando a niveles vibracionales superiores.
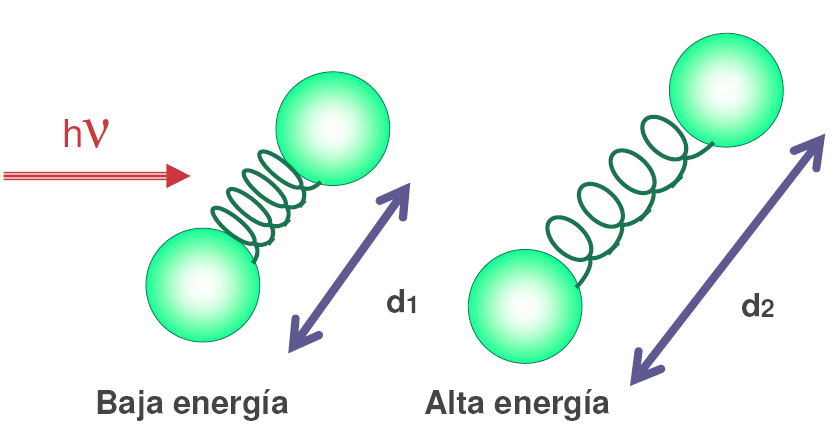
Cada tipo de enlace absorbe radiación infrarroja a una frecuencia distinta, lo que permite determinar que tipo de grupos funcionales posee la molécula en estudio.
Los espectrofotómetros de infrarrojo trabajan en el infrarrojo medio y hacen un barrido desde los 4000 $cm^{-1}$ hasta los 400 $cm^{-1}$
Tradicionalmente, en el eje x de los espectros de infrarrojo se emplea el número de ondas ($\bar{\nu}$, léase "nu barra"') y se define como el inverso de la longitud de onda en cm. $\bar{\nu}=\frac{1}{\lambda}$. En el eje y se representa el porcentaje de radiación transmitida (transmitancia) que se representa por $\%T$. A continuación, se muestra la forma que presenta el espectro de infrarrojos del hexano.
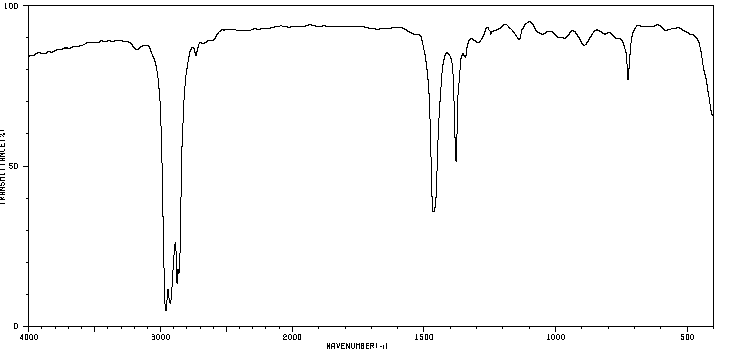
Las bandas representan zonas donde los enlaces de la molécula absorben radiación infrarroja. En las bandas la transmitancia es pequeña y la absorbancia grande.