 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
 Acidez de las aminas
Acidez de las aminas
Los hidrógenos del grupo amino son debidamente ácidos, pudiendo ser arrancados con bases muy fuertes (organometálicos de litio). Por otro lado el par libre del nitrógeno es accesible a la protonación convirtiendo a las aminas en bases aceptables.
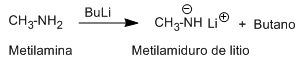
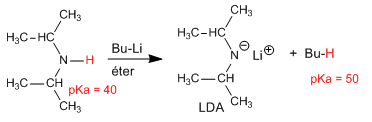
Preparación de LDA
Para la desprotonación de aminas se utilizan bases muy fuertes como los organometálicos de litio. Así, la preparación del diisopropilamiduro de litio (LDA) se realiza a partir de diisopropilamina y buti-litio. El pKa del amoniaco y aminas alifáticas primarias se sitúa en 35, subiendo ligeramente al aumentar el número y tamaño de los sustituyentes.
Comportamiento básico de las aminas
Las aminas actúan como bases a través del par libre del nitrógeno. La protonación del nitrógeno genera las sales de amonio.
Formación de sales de amonio
Las aminas se protonan en medios ácidos formando sales de amonio
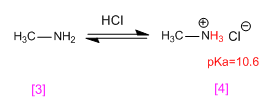
La metilamina [3] se protona transformándose en el cloruro de metilamonio (sal de amonio) [4]. Las sales de amonio son los ácidos conjugados de las aminas y tienen pKas que varían entre 9 y 11.
La basicidad de las aminas depende de los efectos inductivo y estérico. Así, el pKa sube con la longitud de la cadena carbonada (efecto inductivo)
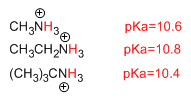
La cadena carbonada cede carga al grupo amino, por efecto inductivo, aumentando su basicidad. La base fuerte tiene un ácido conjugado débil, por tanto, el pka sube. Pero si la cadena es muy voluminosa, comienzan a predominar efectos estéricos, que provocan una disminución del pKa.
YouTube | Miembros del canal Hazte miembro del canal para acceder a todos los vídeos Vídeos para miembros