 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
 Hidrólisis ácida de ésteres
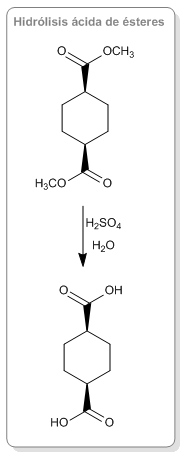
Hidrólisis ácida de ésteres
Los ésteres se hidrolizan formando ácidos carboxílicos y alcoholes cuando se les calienta en medios ácidos o básicos. La hidrólisis de los ésteres es la reacción inversa a la esterificación.
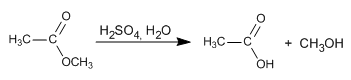
Mecanismo:
Etapa 1. Protonación
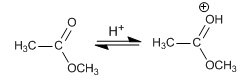
Etapa 2. Ataque nucleófilo del agua
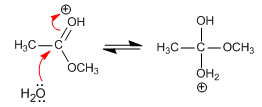
Etapa 3. Equilibrio ácido-base
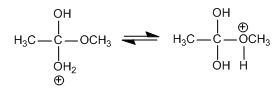
Etapa 4. Eliminación
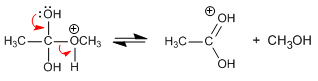
Etapa 5. Desprotonación del ácido
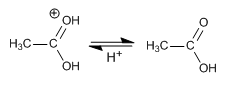
Hidrólisis básica de ésteres o saponificación
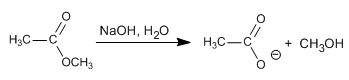
Mecanismo:
Esta reacción transcurre mediante un mecanismo de adición eliminación. En una primera etapa se adiciona el grupo hidróxi al carbonilo del ester, y en la segunda etapa se produce la eliminación de metóxido
Etapa 1. Ataque nucleófilo
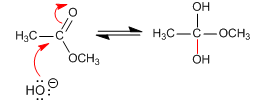
Etapa 2. Eliminación
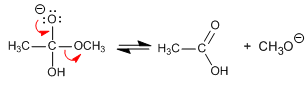
Etapa 3. Equilibrio ácido-base
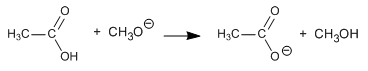
La última etapa, de importante irreversibilidad, hace que la hidrólisis básica sea más efectiva que la ácida. La última etapa desplaza los equilibrios hacia el producto final.
YouTube | Miembros del canal Hazte miembro del canal para acceder a todos los vídeos Vídeos para miembros