 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
El ácido cinámico tiene propiedades fungicidas y es un potente limpiador.
Resulta especialmente indicado para descomponer tejidos necróticos (muertos) y como calmante del dolor.
Fundamentos de la preparación
La reacción de Perkin consiste en la condensación del anhídrido acético con aldehídos aromáticos catalizada por una base débil. En el caso del benzaldehído se obtiene el anhídrido mixto del ácido cinámico y el ácido acético, cuya posterior hidrólisis conduce a los correspondientes ácidos carboxílicos. La geometría trans del ácido cinámico aislado es el resultado de un control termodinámico, que favorece la formación del compuesto más estable.
Reacción de la síntesis
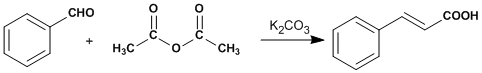
Instrumentación
Equipos para reflujo y para filtración por succión.
Reactivos
Benzaldehído (d 1.044) 6.0 g (inflamable, tóxico)
Anhídrido acético 9.0 g (corrosivo)
Carbonato potásico 2.5 g (corrosivo)
Hidróxido potásico solución 2 M 85 ml (corrosivo)
Eter dietílico 20 ml (inflamable, irritante)
Ácido clorhídrico conc. (corrosivo)
Carbón activo
Procedimiento experimental
En un matraz esférico de 100 ml se introducen 2.5 g de carbonato potásico anhidro, 9 g de anhídrido acético y 6 g de benzaldehído. Acoplar un refrigerante, agitar y calentar suavemente. Se producirá desprendimiento de gases. Una vez que finalice éste, debe llevarse la mezcla a reflujo por espacio de 60 minutos. Entonces, se deja enfriar el crudo de reacción y se vierte lentamente sobre 85 ml de potasa acuosa 2 M con cuidado, pues esta etapa es exotérmica. La solución acuosa que resulta se lava con 20 ml de éter dietílico y se decolora mediante adición de 1 g de carbón activo, calentamiento a 60ºC durante 15 minutos y filtración. Una vez frío el filtrado, se acidula con ácido clorhídrico concentrado hasta pH=2 y se enfría en baño de hielo para completar la precipitación del ácido cinámico. El sólido blanco que resulta se separa por filtración a vacío, se lava con agua fría y se seca, primero por succión y luego en el desecador. Medir el punto de fusión y calcular el rendimiento de la reacción.