 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
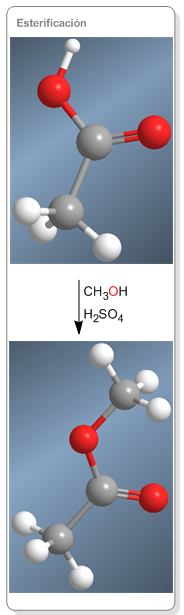 Reacción de esterificación
Reacción de esterificación
Los ésteres se obtienen por reacción de ácidos carboxílicos con alcoholes y está catalizada por ácidos minerales. Otra forma de obtener ésteres es a partir de carboxilatos y haloalcanos mediante una reacción SN2.
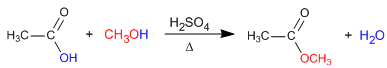
Mecanismo de la esterificación
Al mezclar el ácido y al alcohol no tiene lugar ninguna reacción, es necesaria la presencia de un ácido mineral (H2SO4, HCl) para que la reacción se produzca. Los equilibrios del mecanismo no son favorables y se desplazan hacia el producto final añadiendo exceso del alcohol o bien retirando el agua formada.
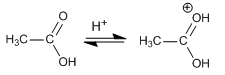
Etapa 1. Protonación del oxígeno carbonílico.
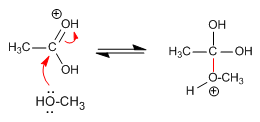
Etapa 2. Adición de metanol
Etapa 3. Equilibrio ácido base
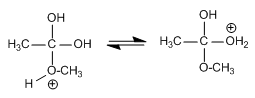
Etapa 4. Eliminación de agua
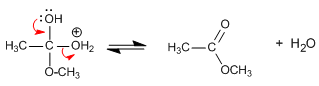
El mecanismo comienza con la protonación del oxígeno carbonílico lo que aumenta la polaridad positiva sobre el carbono y permite el ataque del metanol. Unos equilibrios ácido-base permiten la protonación del -OH que se va de la molécula ayudado por la cesión del par electrónico del segundo grupo hidroxilo.
 Síntesis de ésteres mediante SN2
Síntesis de ésteres mediante SN2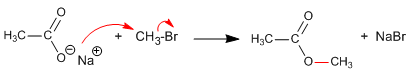
Esta reacción permite formar lactonas macrocíclicas.
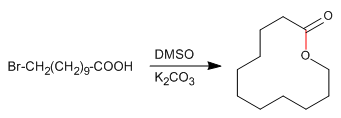
El carbonato de potasio produce un medio básico que desprotona el ácido carboxílico, formando su sal, un buen nucleófilo.
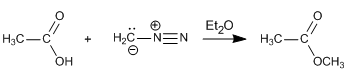
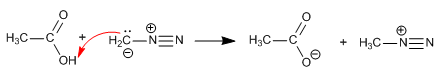
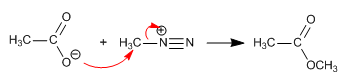
YouTube | Miembros del canal Hazte miembro del canal para acceder a todos los vídeos Vídeos para miembros