¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp.
Más información en www.foroquimico.com
Como vimos en los puntos anteriores, el método retrosintético se basa en romper enlaces de la molécula objetivo para obtener materiales de partida más simples que puedan generarla. La ruptura de un enlace produce dos fragmentos, uno cargado positivamente y otro negativamente. A estos fragmentos se les denomina sintones, y aunque pueden no existir como moléculas reales, nos dan una idea de la forma que tendrá el nucleófilo y electrófilo que debemos utilizar para formar el enlace desconectado. Veamos un ejemplo:
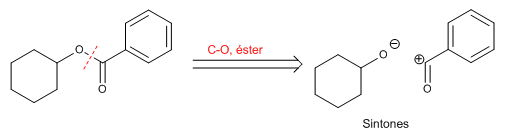
Estos sintones no tienen existencia real, pero pero pueden generarse fácilmente a partir de compuestos orgánicos estables, como pueden ser ciclohexanol y ácido benzoico, llamados equivalentes sintéticos.
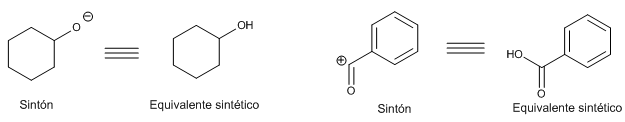
El catión acilo presenta otros equivalentes sintéticos, además del ácido benzoico, como el cloruro de benzoílo o el anhídrido benzoico.
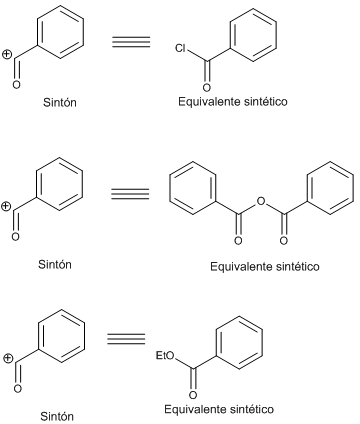
La existencia de varios equivalentes sintéticos permite plantear diversas alternativas sintéticas.
Ruta 1. Reacción entre ciclohexanol y ácido benzoico
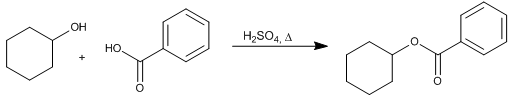
Ruta 2. Reacción entre el ciclohexanol y el cloruro de benzoilo
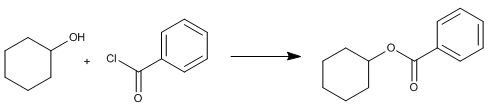
Ruta 3. Reacción entre el ciclohexanol y el anhídrido benzoico
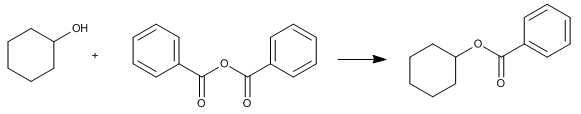
Ruta 4. Reacción entre ciclohexanol y benzoato de etilo (transesterificación)